查看更多

 明星产品
明星产品
 干货推荐
干货推荐
 关注我们
关注我们

扫码关注我们
了解更多信息
芳香烃受体(Aryl hydrocarbon receptor,AhR)是一种由配体激活的转录因子和核受体。AhR可通过多种途径调节病毒的感染和复制,从而为许多病毒提供了生存优势。有研究报道,感染严重急性呼吸综合征冠状病毒2 (SARS-CoV-2)后,AhR被激活以促进病毒复制,表明在SARS-CoV-2感染期间AhR调节可能具有新的治疗作用。然而AhR是否在SARS-CoV-2复制中作为原宿主因子发挥作用,以及AhR是否可成为针对SARS-CoV-2及其变体的广谱抗病毒治疗靶标尚有待深入研究。
2023年5月31日,中国医学科学院医学生物学研究所彭小忠、胡云章及鲁帅尧为共同通讯作者在《Science Advances》(IF=14.957)发表了题为“Aryl hydrocarbon receptor is a proviral host factor and a candidate pan-SARS-CoV-2 therapeutic target”的研究论文。在本研究中,作者发现SARS-CoV-2感染通过干扰IFN-I驱动的抗病毒免疫和上调ACE2受体表达来激活AhR信号并促进病毒复制。药物阻断AhR或敲除AhR可减少SARS-CoV-2及其变体的体外复制。用AhR拮抗剂靶向AhR可显著降低SARS-CoV-2及其变体在体内的复制,并可改善仓鼠由SARS-CoV-2感染引起的肺部炎症。证实了AhR是SARS-CoV-2的原宿主因子,也是针对SARS-CoV-2及其变体(包括Delta和Omicron)以及未来可能出现的其他变体进行抗病毒治疗的候选宿主定向广谱靶标。值得注意的是,研究AhR功能的重要工具——敲除AhR的HepG2细胞株由汉恒生物通过构建Cas9和特异性gRNA慢病毒筛选而来。
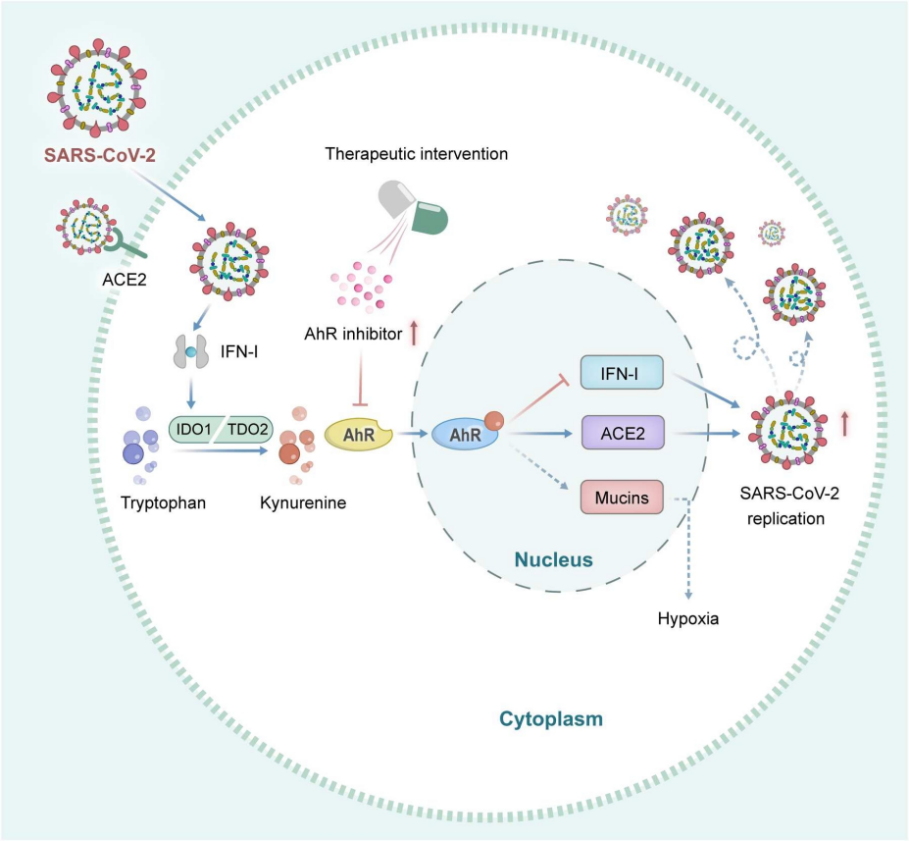
图1. AhR促进SARS-CoV-2复制并作为治疗靶点的示意图
下面我们一起看下本文的具体研究结果:
首先,作者对感染SARS-CoV-2的猕猴肺组织进行了单细胞RNA测序以及感染病毒后的细胞系分析,发现SARS-CoV-2感染可增加AhR上游基因IDO1及下游靶标基因CYP1A1和CYP1B1的表达量。并检测到了IFN和IFN刺激基因的显著上调,同时发现感染病毒可促进Trp向Kyn(AhR内源性配体)的代谢,促进AhR入核,AhR信号通路基因明显上调。利用IFNβ处理细胞可显著增加AhR信号通路基因的表达上调,激活AhR信号传导。综合上述结果,作者认为SARS-CoV-2感染诱导IFN产生,进而促进Trp代谢产生Kyn,促进AhR从细胞质进入细胞核,启动AhR转录靶基因的表达。确定了SARS-CoV-2感染通过IFN-IDO1-Kyn依赖途径激活AhR。
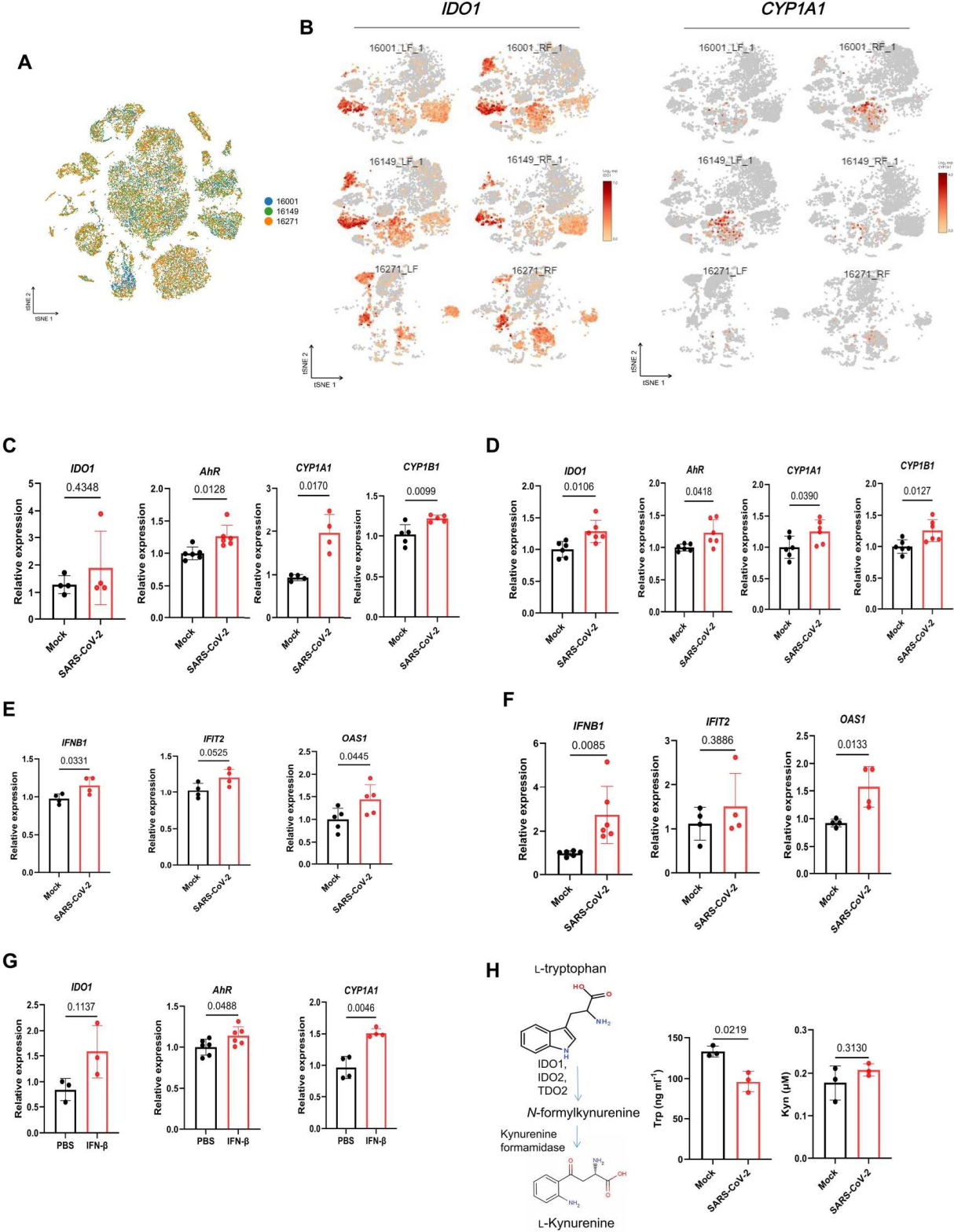
图2. SARS-CoV-2感染激活IFN-IDO-Kyn依赖通路中的AhR信号
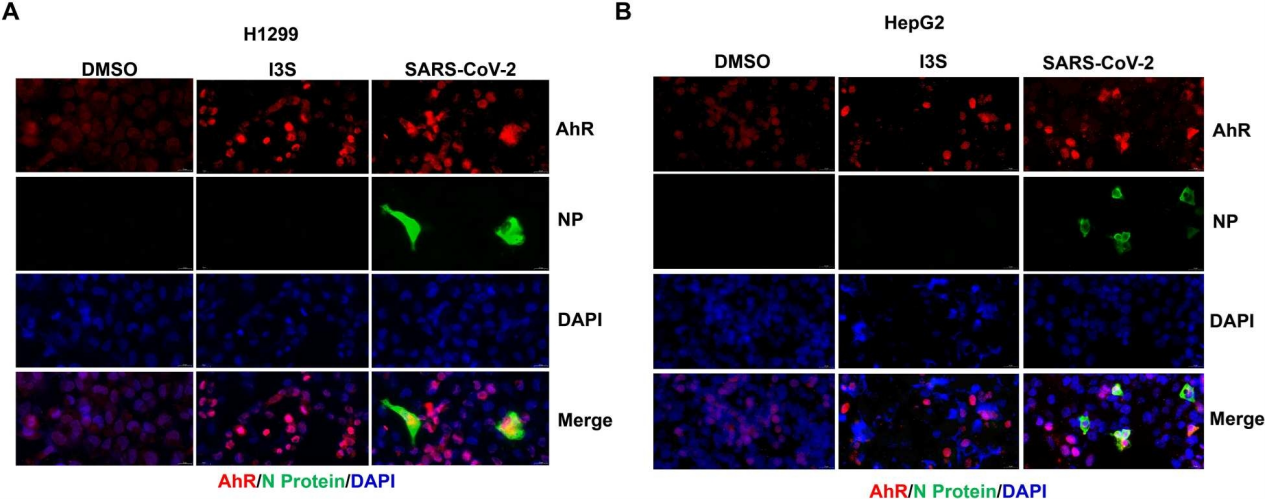
图3. SARS-CoV-2感染促进AhR进入细胞
随后,作者利用SARS-CoV-2感染野生型HepG2和AhR敲除HepG2细胞(AhR−/−HepG2),发现在感染后AhR−/−HepG2中的N蛋白表达水平、荧光强度以及病毒滴度均显著低于野生型HepG2。而使用AhR激动剂增加了野生型HepG2中病毒N蛋白水平和病毒滴度,但无论是AhR激动剂或拮抗剂对AhR−/−HepG2细胞中的SARS-CoV-2复制没有影响。表明AhR是SARS-CoV-2的原宿主因子,对SARS-CoV-2的有效复制至关重要。
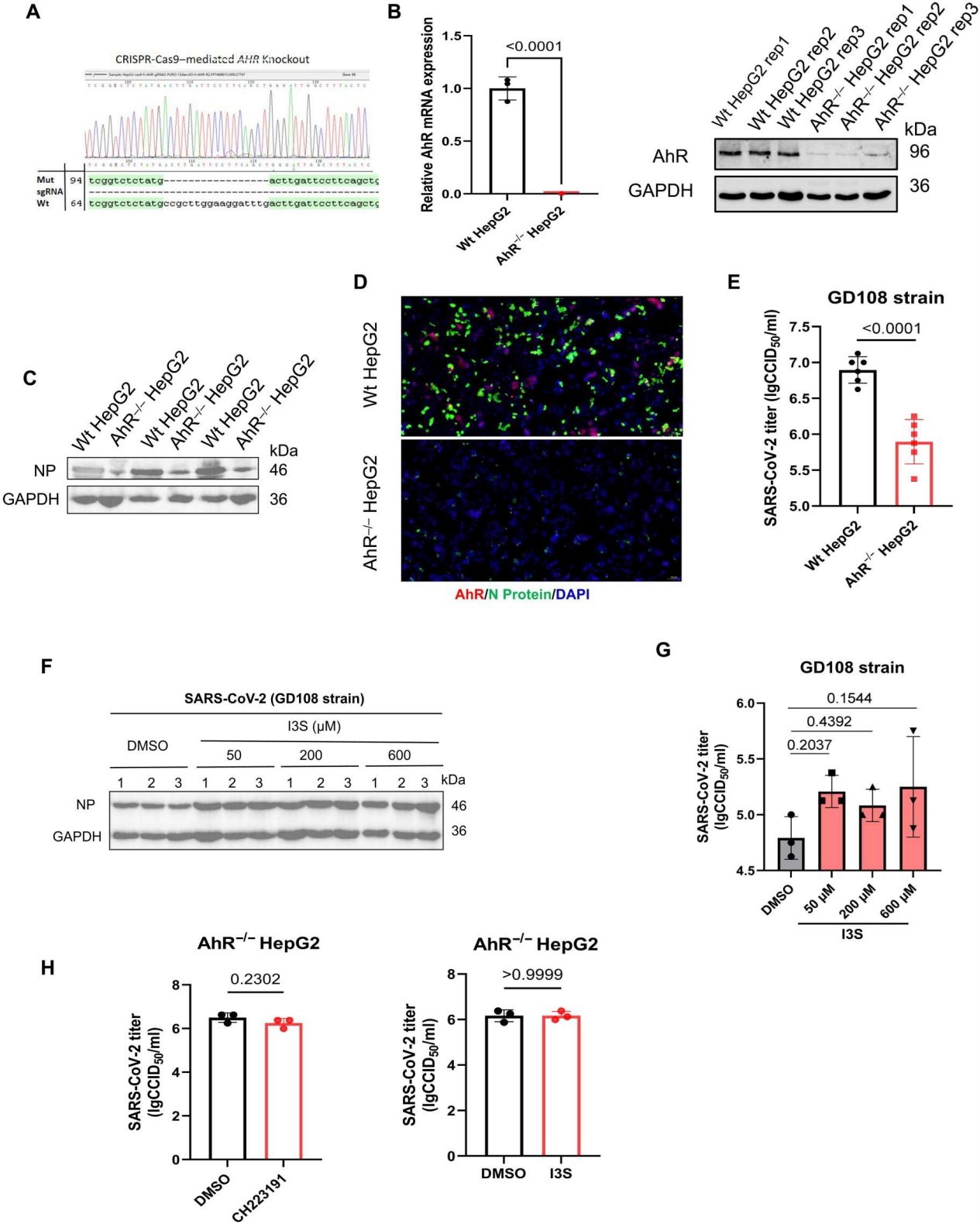
图4. AhR是SARS-CoV-2感染的原宿主因子
在证实AhR是SARS-CoV-2复制所必需后,作者使用AhR拮抗剂CH223191评估了AhR对SARS-CoV-2及其变体的病毒复制的调控作用。作者发现肝癌细胞系H1299、HepG2和Huh7在感染SARS-CoV-2后用CH223191处理,病毒的N蛋白表达被CH223191以剂量依赖性方式显著抑制。随着CH223191浓度的增加N蛋白的荧光逐渐减弱,病毒滴度也显著降低。在人肺癌细胞系Calu-3中也观察到类似的结果。为了研究AhR抑制在哪个阶段干扰病毒感染过程,利用CH223191处理感染SARS-CoV-2不同阶段(病毒进入前预处理、病毒吸附期和病毒内化期)的Huh7细胞。显示CH223191在感染早期对SARS-CoV-2复制没有影响,提示AhR对SARS-CoV-2复制的促进发生在感染后期。综上结果表明,AhR的药理抑制限制了SARS-CoV-2及其变体在体外的复制。
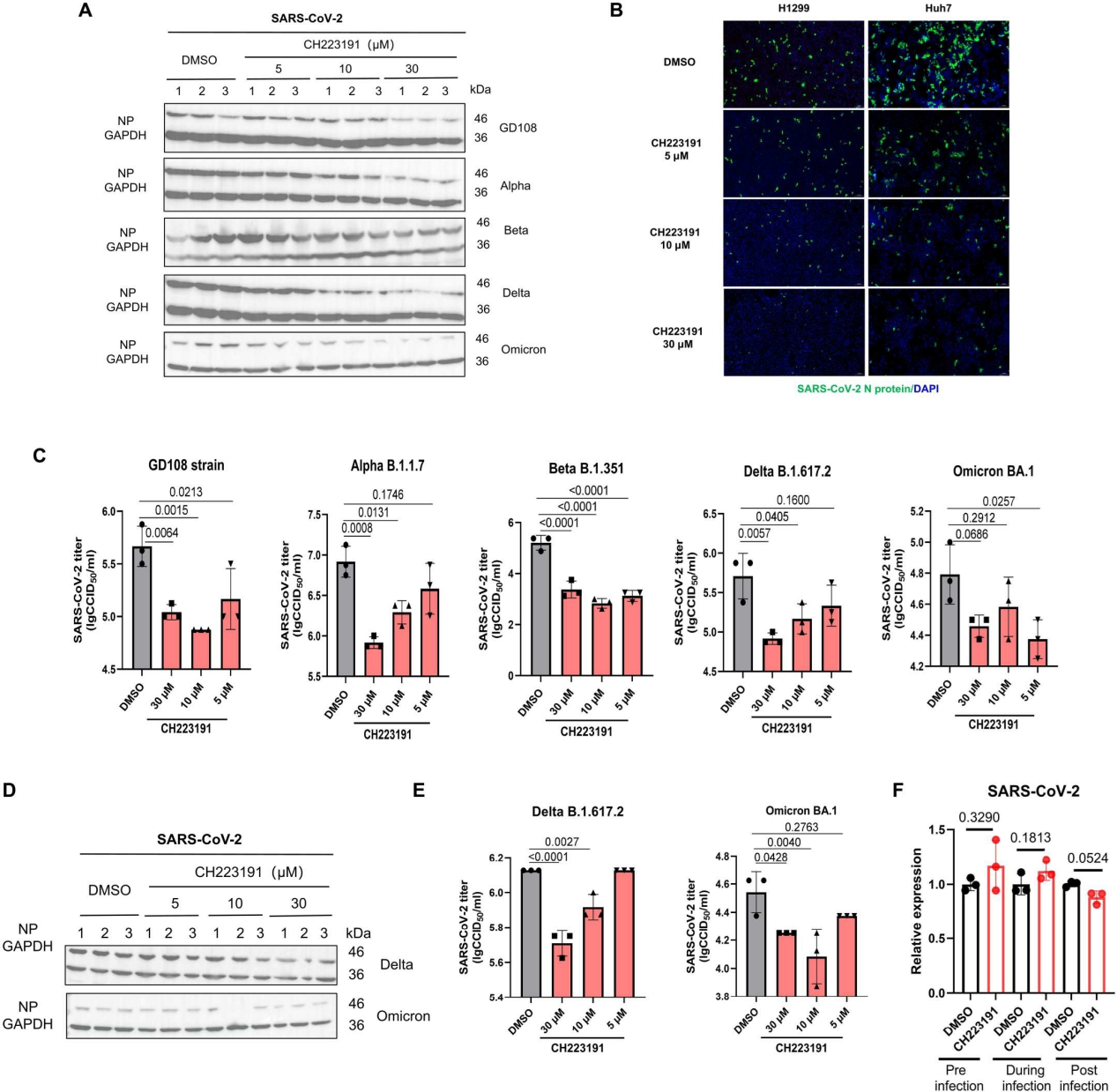
图5. 体外抑制AhR抑制SARS-CoV-2及其变体的复制
接下来,作者对AhR在SARS-CoV-2复制过程中控制抗病毒反应作用进行了研究。利用表达ACE2(介导SARS-CoV-2病毒进入细胞的受体)并可被SARS-CoV-2感染的H1299和HepG2细胞,研究AhR对IFN和ISGs表达的潜在影响。结果显示,抑制AhR增加了H1299中IFN-I和ISGs的表达,降低了SARS-CoV-2病毒RNA水平。在HepG2中也观察到类似的结果。作者认为AhR通过限制IFN-I介导的宿主抗病毒反应来促进SARS-CoV-2的复制。而AhR拮抗剂限制AhR的激活,增强宿主抗病毒反应,从而减少病毒复制。接下来,作者使用SARS-CoV-2感染可正常表达AhR但缺乏IFN表达的非洲绿猴肾细胞(Vero),并用二甲基亚砜DMSO及CH223191处理细胞。结果显示与对照组相比CH223191处理的细胞中SARS-CoV-2复制显著减少。而用IFN-I信号抑制药物处理感染病毒后的细胞中,观察到了病毒复制增加,而抑制AhR病毒复制则会减弱。这些结果证实了SARS-CoV-2引发AhR激活从而抑制IFN-I依赖性反应,促进SARS-CoV-2复制。先前的研究表明病毒复制受到其他不依赖于IFN-I机制的限制,而作者也发现抑制AhR可以减少IFN-I缺陷的Vero细胞中SARS-CoV-2的感染,证实了这一点。这些结果表明,AhR也能通过干扰非IFN-I依赖的抗病毒机制,促进SARS-CoV-2复制。
作为转录因子AhR与ACE2基因的启动子结合,直接调控ACE2的转录,因此对SARS-CoV-2进入细胞至关重要。作者发现ACE2的表达在CH223191或I3S处理后受到影响,表明ACE2的表达受AhR信号通路的调节。另外,在AhR−/−HepG2中ACE2的表达不受病毒感染量影响。相比之下,在感染SARS-CoV-2后H1299和HepG2中ACE2的表达上调,但当AhR被CH223191抑制时,ACE2的表达降低。证实了AhR对ACE2的转录调控作用,ACE2表达上调促进SARS-CoV-2感染,加重肺部病理。
总之,上述实验表明,AhR通过限制IFN-I依赖的抗病毒机制和上调ACE2受体的表达来促进SARS-CoV-2感染、SARS-CoV-2复制和发病机制中的作用,并确定了AhR拮抗剂是COVID-19的候选治疗方法。
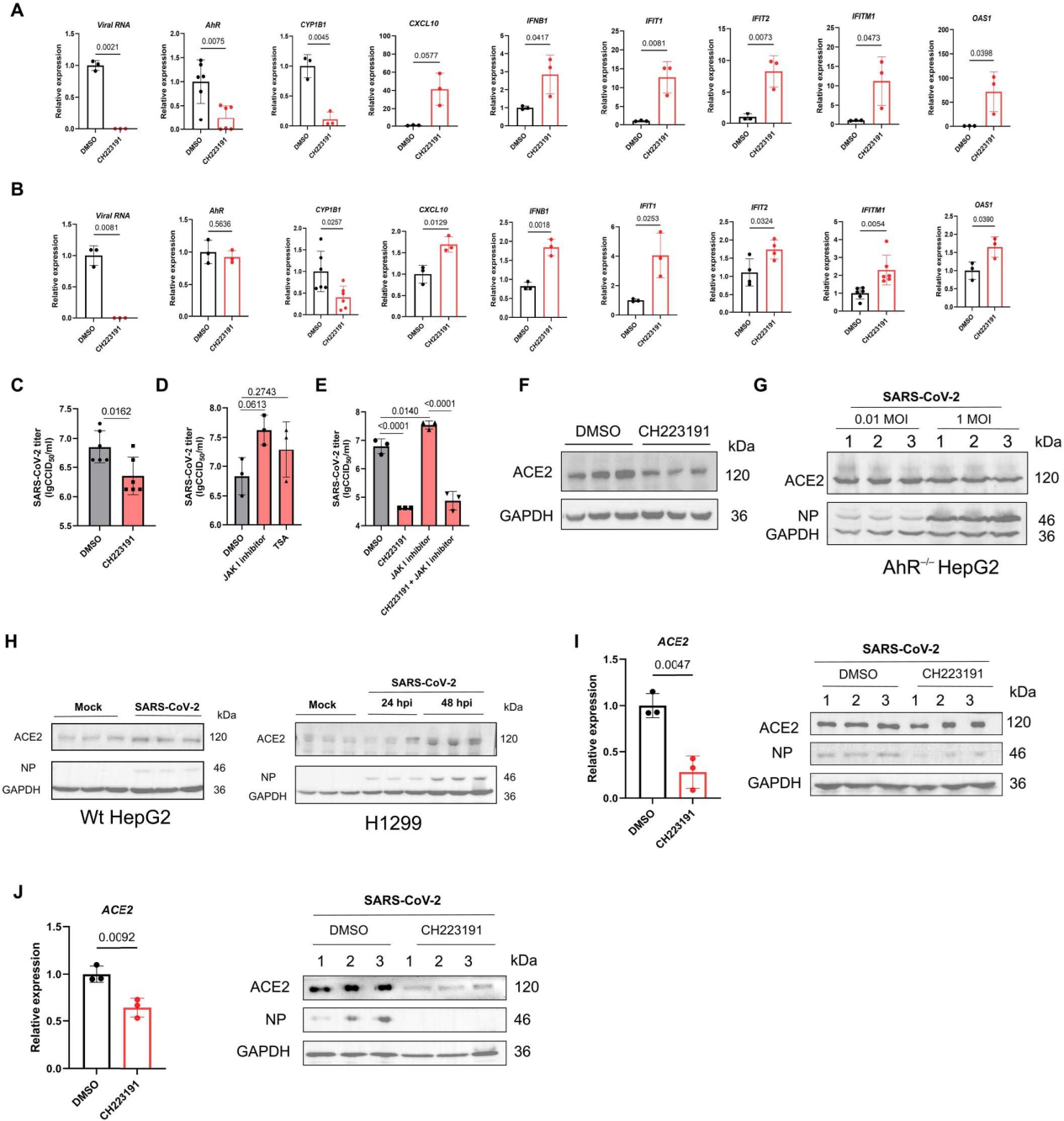
图6. AhR通过限制IFN-1反应和上调ACE2转录来促进SARS-CoV-2复制
最后,作者评估了AhR拮抗剂CH223191对感染SARS-CoV-2及其变体的叙利亚仓鼠的治疗潜力。叙利亚仓鼠对SARS-CoV-2高度敏感,可作为SARS-CoV-2感染模型来评价药物和疫苗的效果。首先,用SARS-CoV-2或其变体感染动物,再腹腔注射CH223191,并对其肺组织进行分析。结果显示,处理组的病毒载量明显下降(>50%)(Omicron变体除外),表明CH223191对AhR的抑制限制了SARS-CoV-2及其变体在体内的复制。同时与对照组相比,CH223191处理组ACE2的表达水平明显降低,而ISGs的表达水平显著升高。且CH223191治疗后,感染仓鼠肺中SARS-CoV-2或其不同变体引起的病理损伤得到改善,主要表现为炎症减轻,肺泡出血减少,肺泡壁变薄,炎症细胞浸润减少。
综上结果表明,抑制AhR可降低ACE2的表达,促进ISGs的表达,以及AhR拮抗剂通过限制病毒复制来部分改善肺病理。总之,这些体内数据有力地支持了AhR信号在SARS-CoV-2复制和发病机制中的作用,并确定AhR拮抗剂是COVID-19的候选治疗方法。
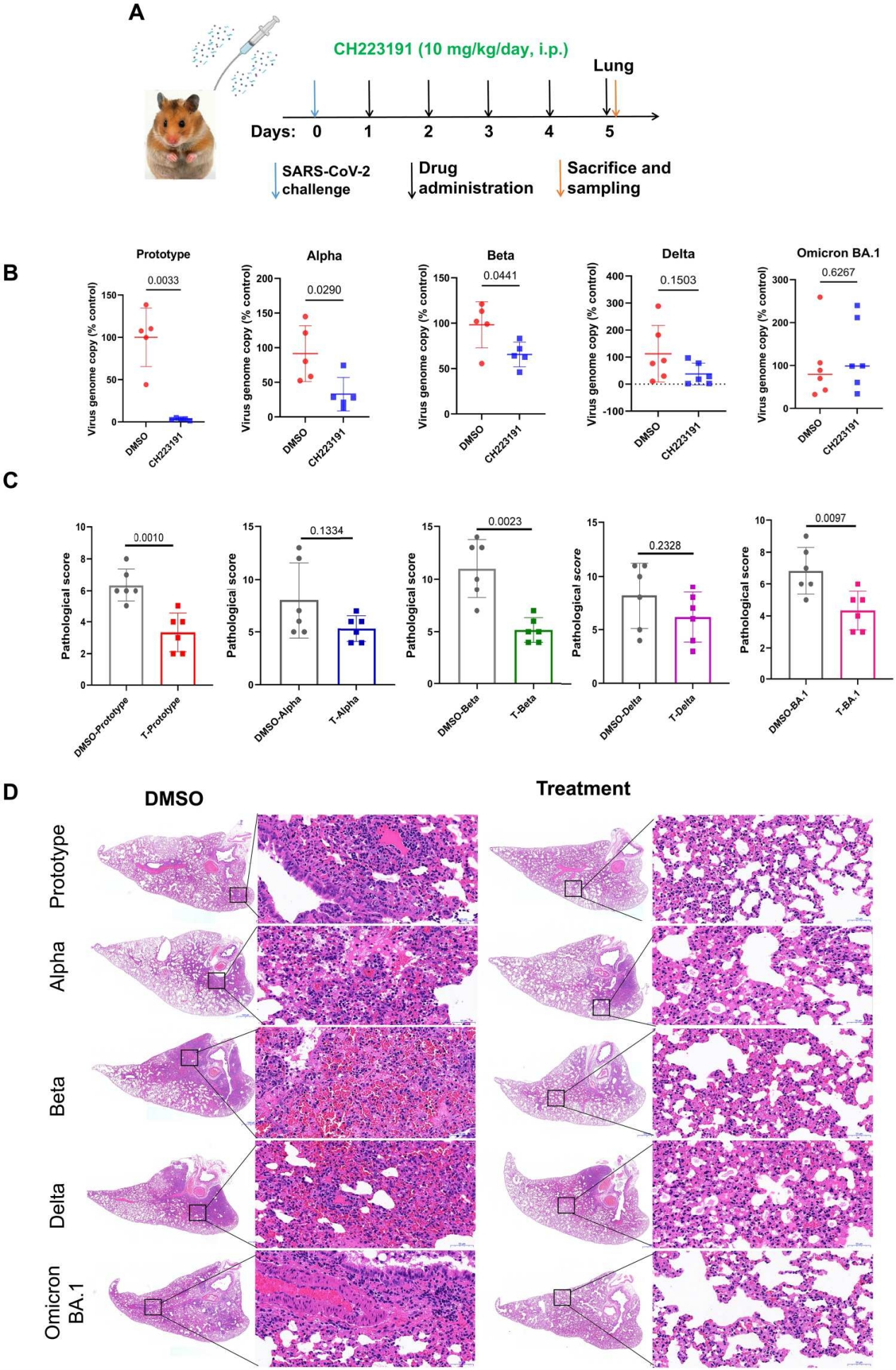
图7. AhR拮抗剂限制SARS-CoV-2复制并改善仓鼠肺炎炎症
综上,本研究探讨了AhR在SARS-CoV-2感染中的作用,并评估了AhR作为宿主靶向抗病毒治疗靶点的潜力。首次提供了AhR抑制作为SARS-CoV-2感染治疗的体内生物学验证。研究发现SARS-CoV-2感染通过干扰IFN-I驱动的抗病毒免疫和上调ACE2受体表达,激活AhR信号并促进病毒复制。药物阻断AhR或敲除AhR可减少SARS-CoV-2及其变体的体外复制。靶向AHR的药物可减少仓鼠体内病毒复制,逆转体内病毒感染引起的肺部炎症病理损伤。以上研究确定了AhR是SARS-CoV-2原宿主因子和抗病毒治疗的候选宿主靶点。作者认为AhR是未来针对SARS-CoV-2及其变体(包括Omicron)的广谱候选治疗靶点。

查看更多

查看更多

查看更多

联系我们

返回顶部